3.
硫酸钾是重要的化工原料,在生产过程中常混有氯化钠杂质。
(1) 用洁净的铂丝蘸取 NaCl 溶液灼烧,火焰呈 色。取少量 K 2 SO 4 溶液,滴入 BaCl 2 溶液,现象是 ,反应的化学方程式是 。
(2) 硫酸钾和氯化钠的部分溶解度数据如有下表。 100℃ 时, NaCl 的溶解度为 g/100g 水; 20℃ 时, 10g 水中最多溶解 K 2 SO 4 g 。
溶解度 (g/100g 水 )
| 温度 (℃) | 0 | 20 | 60 | 100 |
| NaCl | 35.7 | 36.0 | 37.1 | 39.2 |
| K 2 SO 4 | 7.4 | 11.1 | 18.2 | 24.1 |
(3) 某 K 2 SO 4 样品中混有 NaCl 杂质,可利用溶解度差异进行提纯。称取 27.5g 样品进行实验,过程如下:
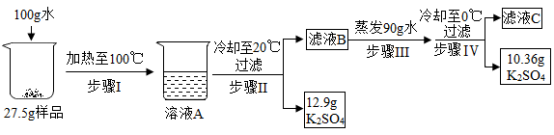
i. 溶液 B 中, K 2 SO 4 ( 选填 “ 达到 ” 或 “ 未达到 ”) 饱和状态。
ii.27.5g 样品中 NaCl 的质量是 g 。
iii. 析上述实验,说明设计步骤 II 对后续操作的作用: 。