
我校化学兴趣小组的同学在一次实验中,将一种金属投入盛有水的烧杯中,发现金属与水剧烈反应,产生大量气泡,根据上述实验现象讨论下列问题:
( 1 )根据你所学的知识,猜想该气体是什么气体(提示:只生成一种气体)
并简述推测的理由: __________________ 。
( 2 )请你设计一个实验验证你的推测(要求:简要完成操作步骤、可能观察到的现象和有关结论)
| 实验操作 | 实验现象 | 结论 |
| 在锥形瓶中加入适量的水,再加入一小块金属后塞上带导管的橡皮塞;收集一试管该气体, _______ | 若有: _______________ | 则是: ________ |
可能是氢气,化学反应前后元素种类不变 移近火焰 气体能燃烧,产生淡蓝色的火焰 氢气
【详解】
( 1 )可能是氢气,根据质量守恒定律,化学反应前后元素种类不变,所以理由是可能是氢气,化学反应前后元素种类不变;
( 2 )方法为验证氢气的步骤,所以为收集一试管气体,移近火焰,若观察到气体能燃烧,产生大蓝色的火焰,则证明是氢气。
登录并加入会员可无限制查看知识点解析
小红用如图装置验证了质量守恒定律,还发现产物中有少量黄色固体。
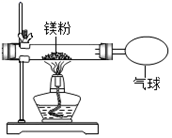
【提出问题】 黄色固体是什么?
【查阅资料】 ①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应生成氨气,该气体能使湿润的红色石蕊试纸变蓝。
【作出猜想】 黄色固体是氮化镁。
【实验探究】 设计实验,验证猜想:
| 实验操作 | 实验现象 | 实验结论 |
| 取燃烧后的产物于试管中,加入少量的_,再将_放在试管口 | ____ | 猜想成立 |
【反思与交流】 空气中氮气的含量远大于氧气的含量,可是镁条在空气中的燃烧产物氧化镁却远多于氮化镁,合理的解释是_。镁在氮气中燃烧的化学方程式为______。
【拓展延伸】 同学们再次查阅资料得知,镁还能在二氧化碳中燃烧,生成一种白色固体氧化物和一种单质,试写出该反应的化学方程式:__。
除去下列物质中的少量杂质,下列选用试剂或方法正确的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | FeSO4溶液 | CuSO4 | 加入过量的锌粉,过滤 |
| B | NaCl | Na2CO3 | 加入过量稀盐酸,蒸发 |
| C | CaCl2溶液 | HCl | 加入过量的Ca(OH)2溶液 |
| D | KCl | MnO2 | 加入足量水溶液、过滤、洗涤、烘干 |
A.A B.B C.C D.D