利用自制多硫化钠可测定空气中氧气含量。实验步骤如下:
① 取 1gNaOH 固体和 1g 硫磺粉末充分研磨后加热,可制得多硫化钠 (Na 2 Sx) ;
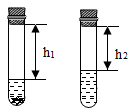
② 待冷却后,取 0.5g 步骤 ① 所得的药品于试管中,加入约 10mL 水,迅速塞紧橡皮塞,如图所示,在试管外做标记 h 1 ,发生的化学反应为: 2Na 2 Sx+O 2 +2H 2 O=_______S↓+4NaOH ;
③ 振荡试管约 1 分钟,将试管倒扣水中,拔下橡皮塞,待试管中液面上升且稳定后,塞好橡皮塞;
④ 从水中取出试管,如图 2 所示,在试管外做标记 h 2 ,下列分析不正确的是
A .步骤 ① 中,充分研磨是为了增大反应物的接触面积
B .步骤 ② 中, S 前面的化学计量数为 2x
C .步骤 ③ 中,试管内液面上升是因为试管中氧气被消耗
D .由该实验可知:空气中氧气含量为
答案
D
【详解】
A 、步骤 ① 中,充分研磨是为了增大反应物的接触面积,正确;
B 、根据质量守恒定律可知,化学反应前后原子的种类和数目不变,反应前 S 的个数为 2x ,反应后 S 的个数也应该为 2x ,因此步骤 ② 中, S 前面的化学计量数为 2x ,故正确;
C 、试管中氧气被消耗,压强减小,液体被压进试管,试管内液面上升,故正确;
D 、进入水的体积即氧气的体积,空气中氧气的含量为 ,故错误;
故选: D 。


