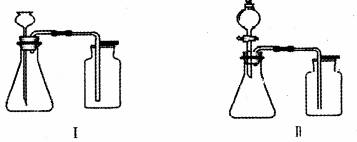KClO 3 制 O 2 常用 MnO 2 作催化剂。某兴趣小组希望寻找到一种廉价易得的 MnO 2 替代品。他们选用的替代品有:碗渣、红砖。其中碗渣和红砖经粉碎后,分成 60 目和 30 目两种颗粒大小不同的粉末,目数越高,颗粒越小。
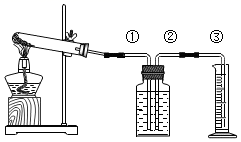
( 1 )实验通过下图装置制取和收集 O 2 ,其中导管位置错误的是 _____ (填序号)。
( 2 )下表是对 KClO 3 分解制 O 2 的催化剂进行研究的实验数据。
| 编号 | KClO 3 质量 /g | 催化剂 | 催化剂质量 /g | 收集 O 2 平均速率 /mL-min -1 |
| 实验 1 | 0.6 | 无 | 0 | 11.8 |
| 实验 2 | 0.6 | MnO 2 | 0.2 | 28.2 |
| 实验 3 | 0.6 | 碗渣粉( 60 目) | 0.2 | 49.1 |
| 实验 4 | 0.6 | 碗渣粉( 30 目) | 0.2 | 23.7 |
| 实验 5 | 0.6 | 红砖粉( x 目) | 0.2 | 28.3 |
| 实验 6 | 0.6 | 红砖粉( y 目) | 0.2 | 21.1 |
①该实验研究了 _____ (填字母)这些因素对收集 O 2 速率的影响。
A 催化剂种类 B 催化剂颗粒大小 C 催化剂质量
②实验 3 、 4 可得出催化剂目数与反应分解速率的关系是:其他条件相同时, _____ 。根据以上规律,请填出实验 5 、 6 中的数据 x= _____ , y= _____ 。
②表中所列催化剂的催化效果最佳的是实验 _____ 。但由于这种物质在通常条件下难以粉碎,故选择实验 _____ 的物质做 MnO 2 的替代品是较为理想的,请写出这种物质催化分解 KClO 3 的化学反应方程式 _____ 。
答案
① AB 催化剂目数越大,反应速率越快 60 30 3 5 2KClO 3 2KCl+3O 2 ↑
【详解】
( 1 )实验通过下图装置制取和收集 O 2 ,其中导管位置错误的是 ①,氧气密度小于水的密度,气体短进长出,入口管过长,故选:①。
( 2 ) ①该实验变量为催化剂种类,以及催化剂颗粒大小,研究了催化剂种类、催化剂颗粒大小这些因素对收集 O 2 速率的影响,故填: AB 。
②实验 3 、 4 可得出催化剂目数与反应分解速率的关系是:其他条件相同时,催化剂目数越大,反应速率越快,为了比较碗渣粉和红砖粉催化效率的强弱,颗粒大小需相同, x 和 y 一个是 30 一个是 60 ,实验 5 生成氧气平均速率大于实验 6 ,故实验 5 目数大于实验 6 ,故 x= 60 , y= 30 ,故填:催化剂目数越大,反应速率越快; 60 ; 30 。
②实验 3 生成氧气速度最快,故表中所列催化剂的催化效果最佳的是实验 3 ,但由于碗渣粉在通常条件下难以粉碎,故选择实验 5 的物质做 MnO 2 的替代品是较为理想的,因为除了碗渣粉和二氧化锰,实验 5 生成氧气速度最快,红砖粉催化分解 KClO 3 的化学反应方程式 2KClO 3 2KCl+3O 2 ↑ ,故填: 3 ; 5 ; 2KClO 3
2KCl+3O 2 ↑ 。

 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
 2H2O+O2↑
2H2O+O2↑