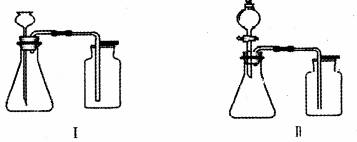根据下列实验装置图填空:(填入相应的选项如 A 、 B…… )
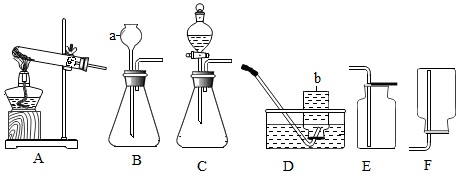
( 1 )写出图中标示的仪器名称: a _____ b _____
( 2 )兴趣小组在实验室用双氧水和二氧化锰制取一瓶相对纯净的氧气,写出反应的化学方程式 _____ ,制取装置组合为 _____ ,当 _____ 以证明收集到氧气已满。
( 3 )兴趣小组集满氧气后进行实验,发现氧气不纯,原因可能是 _____ 。
( 4 )兴趣小组还需要一瓶干燥的氧气,如图方框处可以选 _____ 收集装置,同时装置 C 中制得的氧气有少量水蒸汽,可用 _____ 除去水蒸气,该物质俗称 _____ 反应基本类型为 _____

( 5 )兴趣小组用氯酸钾制取氧气时,发现没有二氧化锰,于是就用高锰酸钾代替(已知高锰酸钾 KMnO 4 )加热反应后生成固体锰酸钾( K 2 MnO 4 )固体二氧化锰和氧气,试回答:
①该反应中二氧化锰属于 _____ ,反应基本类型属于 _____ 。
②反应结束后,对剩余的固体物质进行分离提纯,兴趣小组查阅资料,含钾的盐类化合物均溶于水,二氧化锰不溶于水;
( 6 ) ①实验室可用 FeS (固体)和盐酸反应制得硫化氢( H 2 S )气体和氯化亚铁,已知 H 2 S 气体可溶于水,密度比空气大,请问:若要制取 H 2 S ,应选用如图中 _____ (填 A 或 B 或 C )作为发生装置,该装置的优点是 _____ 反应的化学方程式为 _____ 其中 FeS 读作 _____ 。
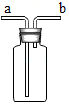
②由于硫化氢气体有剧毒,故一般采用如图所示装置进行收集。收集时,硫化氢气流从 _____ (填 “a” 或 “b” )进入。
③专家提醒:下水道硫化氢气体泄漏时,可以用湿毛巾捂住鼻子做好防护,井向高处转移,这种做法的理由是 _____ 。
答案
长颈漏斗 集气瓶 2H 2 O 2 2H 2 O+O 2 ↑ BD 或 CD 集气瓶口有大气泡冒出时 没有等到气泡均匀连续冒出就收集、集气瓶中的水没有装满等 E 氢氧化钠固体 火碱 烧碱或苛性钠 分解反应 催化剂 分解反应 B 或 C 方便加液体药品或可以控制反应的速率 FeS+2HCl = FeCl 2 +H 2 S↑ 硫化亚铁 a H 2 S 气体可溶于水
【解析】
( 1 )图中标示 a的仪器名称是长颈漏斗;图中标示b的仪器名称是集气瓶;
( 2 )过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为: 2H 2 O 2 2H 2 O+O 2 ↑ ;用双氧水和二氧化锰制氧气,反应物的状态是固体和液体,不需要加热,可用 B 或 C 作为发生装置,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净,收集装置选用 D 。在实验室用双氧水和二氧化锰制取一瓶相对纯净的氧气,制取装置组合为 BD 或 CD ;氧气集满的现象是集气瓶口有大气泡冒出;
( 3 )兴趣小组集满氧气后进行实验,发现氧气不纯,原因可能是:没有等到气泡均匀连续冒出就收集、集气瓶中的水没有装满等;
( 4 )兴趣小组还需要一瓶干燥的氧气,如图方框处可以选向上排空气法收集,收集装置选用 E ;同时装置 C 中制得的氧气有少量水蒸汽,氢氧化钠固体具有吸水性,可用氢氧化钠固体除去水蒸气,氢氧化钠俗称火碱、烧碱或苛性钠;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,该反应是由一种物质分解生成两种物质,属于分解反应;
( 5 )兴趣小组用氯酸钾制取氧气时,发现没有二氧化锰,于是就用高锰酸钾代替(已知高锰酸钾 KMnO 4 )加热反应后生成固体锰酸钾( K 2 MnO 4 )、固体二氧化锰和氧气;该反应中二氧化锰属于催化剂,反应基本类型属于分解反应;
( 6 ) ①根据“实验室可用 FeS (固体)和盐酸反应制得硫化氢( H 2 S )气体和氯化亚铁 ”可知,该反应的反应物是固体和液体,不需要加热,发生装置可选用 B 或 C ; B 装置中长颈漏斗可随时添加液体, C 装置中的分液漏斗可控制液体的滴加速率,可以控制反应的速率,该装置的优点是:方便添加液体药品或可以控制反应的速率;反应的化学方程式为: FeS+2HCl = FeCl 2 +H 2 S↑ ;其中 FeS 读作硫化亚铁;
②由于硫化氢气体有剧毒,故一般采用如图所示装置进行收集。收集时,硫化氢气体从a(长)管进入,因为硫化氢气体的密度比空气大;
③专家提醒:下水道硫化氢气体泄漏时,可以用湿毛巾捂住鼻子做好防护,并向高处转移,这种做法的理由是: H 2 S 气体可溶于水。
【点睛】
本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥、反应类型、注意事项等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。

 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
 2H2O+O2↑
2H2O+O2↑