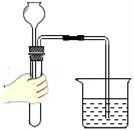
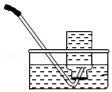
根据如图回答问题。
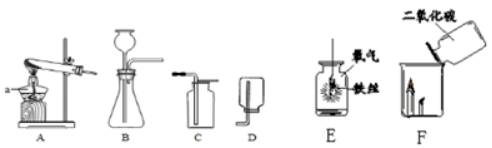
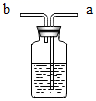
( 1 )仪器 a 的名称是 _____ 。
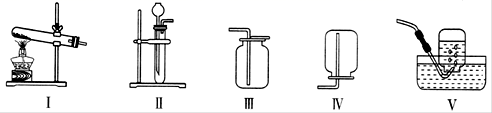
( 2 )实验室用高酸钾制取氧气的化学方程式是: _____ ,选用的收集装置是 _____ ,试管口塞棉花的作是 _____ 。如图 E 所示,铁丝与与气反应的化学方程式是 _____ ,集气瓶底装水的作用是 _____ 。
( 3 )实验室制取二氧化碳的化学方程式是 _____ 。
( 4 )选用的发生装置是 _____ ,其装置用来制取氢气的化学方程式 _____ 。
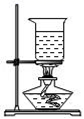
( 5 )如图 F 所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自上而下一次熄灭,说明二氧化碳具有的性质是 _____ 、 _____ 。
答案
酒精灯 2KMnO 4 ![]() K 2 MnO 4 +MnO 2 +O 2 ↑ C 为了防止高锰酸钾粉末进入导管 3Fe+2O 2
K 2 MnO 4 +MnO 2 +O 2 ↑ C 为了防止高锰酸钾粉末进入导管 3Fe+2O 2 ![]() Fe 3 O 4 为了防止铁的熔化物溅落,而炸裂集气瓶 CaCO 3 +2HCl = CaCl 2 +H 2 O+CO 2 ↑ B Zn+H 2 SO 4 = ZnSO 4 +H 2 ↑ 二氧化碳既不能燃烧也不能支持燃烧 二氧化碳的密度比空气的密度大
Fe 3 O 4 为了防止铁的熔化物溅落,而炸裂集气瓶 CaCO 3 +2HCl = CaCl 2 +H 2 O+CO 2 ↑ B Zn+H 2 SO 4 = ZnSO 4 +H 2 ↑ 二氧化碳既不能燃烧也不能支持燃烧 二氧化碳的密度比空气的密度大
【解析】
( 1 )由图可知,仪器 a 的名称是酒精灯,故填酒精灯。
( 2 )高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,故反应的化学方程式写为: 2KMnO 4 ![]() K 2 MnO 4 +MnO 2 +O 2 ↑ ;
K 2 MnO 4 +MnO 2 +O 2 ↑ ;
氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,故填 C ;
加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管污染气体,故填为了防止高锰酸钾粉末进入导管;
铁和氧气在点燃的条件下生成四氧化三铁,故反应的化学方程式写为: 3Fe+2O 2  Fe 3 O 4 ;
Fe 3 O 4 ;
集气瓶底装水的作用是:为了防止铁的熔化物溅落,炸裂集气瓶,故填为了防止铁的熔化物溅落,炸裂集气瓶。
( 3 )碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,故反应的化学方程式写为: CaCO 3 +2HCl = CaCl 2 +H 2 O+CO 2 ↑ 。
( 4 )实验室制取 CO 2 ,是在常温下,用大理石或石灰石和稀盐酸制取的,应选择固液常温发生装置,故填 B ;
实验室是用锌粒和稀硫酸在常温下反应生成硫酸锌和氢气,故反应的化学方程式写为: Zn+H 2 SO 4 = ZnSO 4 +H 2 ↑ 。
( 5 )如图 F 所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自上而下一次熄灭,说明二氧化碳具有的性质是:二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大,故填二氧化碳既不能燃烧也不能支持燃烧,二氧化碳的密度比空气的密度大。
【点睛】
制取气体时,选择气体发生装置的依据是反应条件和反应物的状态,选择收集装置的依据是被收集气体的密度与溶解性。





 2H2↑+O2
2H2↑+O2 CO+H2
CO+H2 2H2↑+O2↑
2H2↑+O2↑